MSI 연구실은 마이크로바이옴(microbiome)이 숙주의 면역시스템 발달에 미치는 영향을 연구하고 있습니다. 오랜 세월에 걸친 공진화 과정을 통해 숙주와 공생 관계를 이루게 된 마이크로바이옴은 다양한 신체 기관의 정상적인 발달과 기능 유지에 영향을 미치는 것으로 알려져 있습니다. 이들과의 관계에 있어서 최전선에 위치한 숙주 면역시스템이 미생물과 영향을 주고받으며 항상성을 유지하기 위한 기작을 장내 T세포의 분화와 기능을 중심으로 밝히고자 하며, 이러한 균형이 깨졌을 때 발생하는 질병, 그리고 이 과정에 영향을 미치는 주요 공생 세균들의 역할 및 생존전략을 연구하는 것을 목표로 하고 있습니다.
1. 마이크로바이옴 대사체에 의한 면역시스템 조절
MSI 연구실은 장내 마이크로바이옴과 숙주 면역계 간의 상호작용을 탐구하며, 특히 마이크로바이옴 유래 대사체(metabolome)가 면역 항상성 유지와 염증 조절에 미치는 영향을 중점적으로 연구합니다. 장내 미생물은 우리가 섭취하는 식이 성분을 분해하여 다양한 대사산물을 생성하며, 이들 대사체는 숙주의 면역세포와 신경세포에 신호를 전달함으로써 면역 반응을 조절하고 조직 항상성을 유지하는 데 핵심적인 역할을 수행합니다. 최근 연구에 따르면, 이러한 대사체들은 염증성 장질환(IBD), 자가면역 질환, 대사 질환, 심지어 신경퇴행성 질환의 발병 및 진행에 영향을 줄 수 있음이 밝혀지고 있습니다. 우리 연구실은 장내 미생물과 식이, 면역계 간의 복합적 상호작용을 분자 수준에서 이해함으로써, 차세대 마이크로바이옴 기반 면역 조절 전략을 개발하고 미생물 기반 치료제 개발을 통한 만성 질환 극복을 목표로 하고 있습니다.
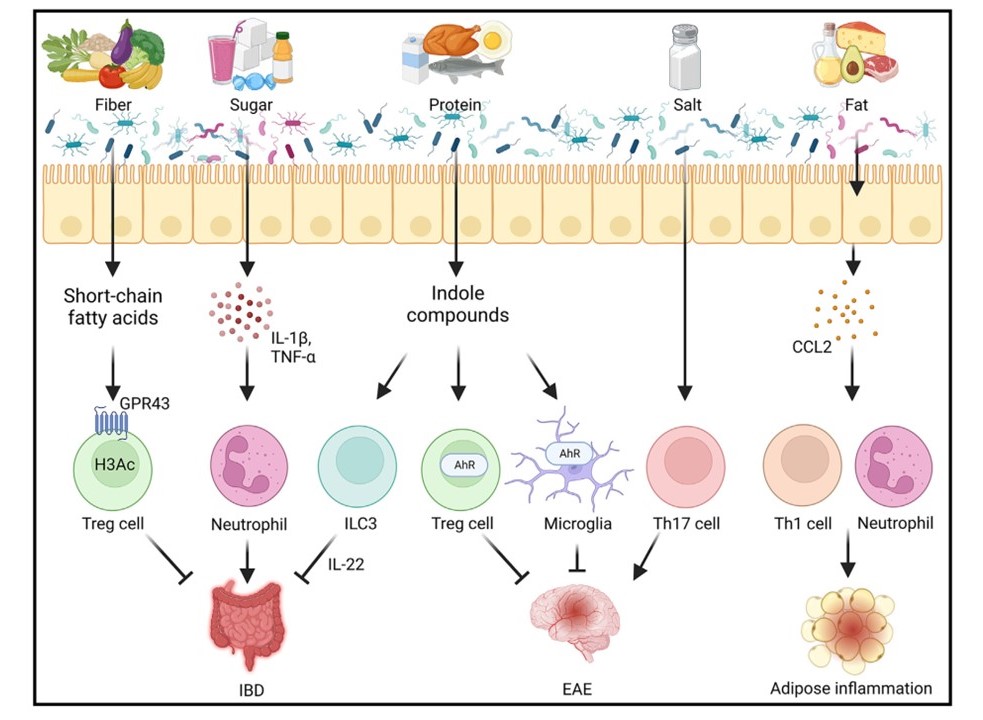
식이 성분-미생물-면역 축의 분자적 연결고리
Arifuzzaman et al., 2024, Immunity
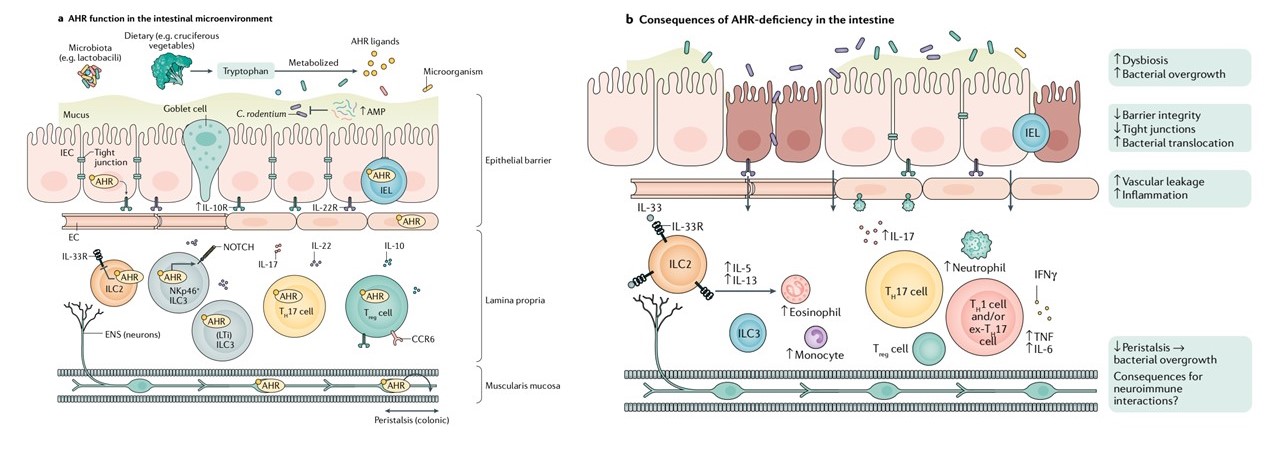
AHR(aryl hydrocarbon receptor) 신호와 장내 면역 항상성
Stockinger et al., 2021, Nat Rev Gastro
2. 마이크로바이옴과 장내 항체 반응의 상호작용
장과 같은 점막 조직에서 상시적으로 분비되고 있는 IgA 항체는 병원균의 침입을 차단하는 동시에 다양한 공생균의 정착과 생리적 기능을 조절하는 것으로 알려져 있으며, 역으로 IgA를 생산하는 B세포의 분화는 장내 세균에서 유래한 항원과 대사물의 영향을 받습니다. 장내 환경 변화에 따라 조절되는 IgA 반응이 미생물과의 공생에 미치는 영향을 밝히고, 공생균에 의해 유도된 항체 반응이 숙주의 장내 면역 항상성을 유지하고 병원균의 침입을 차단하는 메카니즘을 연구하고 있습니다.

장에서의 T세포 의존적 IgA 반응
(edited by BioRender)
3. 식이에 의한 마이크로바이옴의 변화가 숙주 대사시스템에 미치는 영향
숙주가 섭취하는 음식은 마이크로바이옴의 구조와 기능을 결정짓는 중요한 요소 중의 하나입니다. 고지방, 저섬유질로 특징 지어지는 서구화된 식단은 장내 마이크로바이옴의 다양성을 감소시키고 비만, 당뇨와 같은 각종 대사질환을 유도하는 세균의 증식을 촉진하는 것으로 알려져 있습니다. 일시적인 식이 변화조차 장내 미생물의 구성을 단기적으로 변화시킬 수 있는 것으로 보이나, 장기적인 식습관으로 인해 형성된 보다 안정된 마이크로바이옴의 구조는 상대적으로 바꾸기 어려우며, 이와 같은 장기 구조에 영향을 미칠 수 있는 요인들과 개인별로 나타나는 독특한 미생물 구성을 결정짓는 요인에 대해서는 알려진 바가 매우 적습니다. 숙주의 대사기능에 영향을 미치는 개별 세균을 중심으로 이들이 식이에 따른 환경 변화에 적응해 나가는 기작을 이해하고, 이들 세균과의 공생관계가 손상되었을 때 나타날 수 있는 질환 기작을 연구함으로써, 숙주의 건강을 위해 마이크로바이옴의 구조를 보다 효과적으로 조절할 수 있는 길을 찾고자 합니다.

장내 세균이 대사질환에 미치는 영향
(Lee and Park, 2022, J Microbiol)
4. 마이크로바이옴-장-뇌 축에 의한 파킨슨 병 조절 기전 연구
파킨슨병 환자 마이크로바이옴 분석을 통해 파킨슨병 증상 발현에 있어서 장내 미생물의 역할을 검증하고 장-뇌 축을 통한 신경염증 발생 기전을 연구하고 있습니다.

(Tansey et al., 2022, Nat Rev Immunol)
5. 마이크로바이옴에 의한 조직 macrophage의 기능 조절 및 역할 규명
Macrophage는 식균작용을 통해 병원균이나 죽어가는 세포의 잔해를 제거하고, 항원제시를 통해 T세포와 같은 면역세포의 분화와 기능을 조절하는 것으로 알려져 있습니다. 그러나 신체의 각 조직에서 주요 생리 기능을 조절하는 조직 특이적 macrophage의 역할이 주목받고 있습니다. 장, 지방조직, 뇌 조직 등에 분포하는 macrophage가 장내세균이 분비하는 다양한 인자들에 의해 조절되어 비만과 같은 각종 만성 질환을 완화시키거나 촉진하는 원리를 규명하고자 합니다.

Tissue-specific macrophage의 기능
(Mass et al., 2023, Nat Rev Immunol)

MAMP의 일종인 세균 flagellin에 의해 유발된 장 dendtritic cell 및 macrophage의 변화
6. 마이크로바이옴에 의한 T세포 분화 조절
장에 분포하고 있는 조절T세포는 크게 두 가지로 분류할 수 있습니다. CD4+ T세포와 마찬가지로 흉선에서 분화된 후 장으로 이동하는 조절T세포는 자연 조절T세포(natural Treg, nTreg)로 불리며, 장으로 이동한 CD4+ T세포에서 Foxp3가 발현되어 분화되는 조절T세포는 peripherally induced Treg (pTreg 또는 iTreg)으로 불립니다. 따라서 장에서 기능하는 조절T세포는 nTreg과 pTreg으로 구성됩니다. 장 점막은 pTreg의 분화를 촉진할 수 있는 환경을 이루고 있으며, 장 내부에 위치한 미생물과 음식물을 흡수하여 항원을 제시하는 수지상세포가 중심적인 역할을 수행하고 있습니다. 이들은 항원 제시뿐만이 아니라 다양한 사이토카인과 비타민A 대사산물인 retinoic acid를 생성하여 조절T세포의 분화를 촉진합니다. 대장에 위치하고 있는 조절T세포들의 T세포 수용기(T cell receptor)는 공생세균으로부터 유래한 항원에 특이적으로 반응하는 것으로 알려져 있습니다. 또한 공생세균으로부터 유래한 다양한 물질들 또한 조절T세포의 분화를 촉진합니다.
특이하게도 장에 분포한 조절T세포의 일부가 Th17세포의 분화와 관련된 RORγt를 발현하고 있다는 것을 발견하게 되었으며, 장내 마이크로바이옴이 이러한 RORγt+ Treg의 분화를 유도한다는 것이 밝혀졌습니다. 장 점막은 외부 환경과 물질에 노출되어 있기 때문에 항시적으로 Th2세포에 의한 면역 반응이 활성화 될 수 있는 조건을 갖추고 있습니다. 그러나 장에 서식하는 마이크로바이옴에 의해 RORγt+ Treg이 분화되어 Th2세포를 활성화시키는 수지상세포를 억제함으로써, 과도한 Th2 면역반응이 질병으로 이어지는 것을 차단할 수 있게 됩니다. 그러나 항생제 등에 의해 마이크로바이옴의 구조나 기능에 변화가 일어나는 경우, RORγt+ Treg의 분화가 정상적으로 이루어지지 않으면서 Th2 면역반응이 과도하게 증폭되면 궤양성 대장염 (ulcerative colitis)과 같은 질환으로 이어지게 됩니다.
본 연구실에서는 T세포의 분화에 영향을 미치는 주요 공생균과 그 대사물질을 발굴하고 그 작용 기전을 규명하고자 합니다.

마이크로바이옴에 의한 T세포 분화
(Ohnmacht & Park et al., 2015, Science)
